今日頭條
加科思中美雙報新藥獲批IND。加科思藥業P53 Y220C激活劑JAB-30300獲FDA批準IND申請,即將在美國開展用于治療晚期實體瘤的I/IIa期臨床。JAB-30300對P53 Y220C突變蛋白具有高親和力,已在臨床前多種腫瘤模型中顯示出消退腫瘤(包括胃癌、卵巢癌、乳腺癌和肺癌等)的潛力;JAB-30300也有潛力與化療或致癌蛋白抑制劑聯合用藥,為患者帶來更多治療方案。加科思計劃同時在中國申報IND。
國內藥訊
1.科倫博泰ADC擬納入第4項突破性認定。科倫博泰TROP2靶向ADC創新藥SKB264獲CDE擬納入第4項突破性認定,用于治療既往未接受過系統治療的不可手術切除的局部晚期、復發或轉移性PD-L1陰性三陰性乳腺癌(TNBC)患者。此前,該新藥已被CDE納入三項突破性療法認定:局部晚期或轉移性三陰乳腺癌,EGFR-TKI治療失敗的局部晚期或轉移性EGFR突變非小細胞肺癌,以及局部晚期或轉移性HR+/HER2-乳腺癌。
2.齊魯組合抗體宮頸癌Ⅱ期臨床積極。齊魯制藥在ESGO2024年會上公布PD-1/CTLA-4組合抗體艾帕洛利托沃瑞利單抗注射液(QL1706)治療宮頸癌的Ⅱ期臨床(DUBHE-C-206)積極結果。該項研究納入一線含鉑化療±貝伐珠單抗失敗且未接受過免疫治療的復發/轉移宮頸癌患者。數據顯示,獨立評價委員會(IRC)評價的QL1706客觀緩解率(ORR)為33.8%;疾病控制率(DCR)為64.9%。臨床中,≥3級TRAE發生率為24.3%。
3.深信mRNA疫苗上美國Ⅰ期臨床。深信生物二價RSV mRNA疫苗IN006在Clinicaltrials.gov網站上注冊一項美國Ⅰ期臨床,計劃入組200例健康受試者,評估IN006的安全性、耐受性和免疫原性。IN006采用該公司具有自主知識產權的LNP遞送系統和mRNA技術平臺,以及自主設計和篩選的融合前構象的F蛋白。在臨床前研究的動物攻毒模型中,IN006已顯示出積極的保護效果,以及良好的安全性。
4.荃信呼吸疾病單抗獲批兩項IND。荃信生物自主研發的1類生物制品QX007N注射液獲國家藥監局兩項臨床默示許可,即將開展用于治療慢性阻塞性肺疾病(COPD)及哮喘兩項適應癥的新藥研究。QX007N是一款重組人源化IL-33單抗,通過與IL-33結合,阻斷IL-33與其受體的結合引起的炎癥級聯反應,從而達到治療效果。
5.恩凱賽藥NK細胞療法報IND。上海恩凱賽藥1類新藥“NK042細胞注射液”的臨床試驗申請獲CDE受理。NK042是一種經過工程修飾的表達多種激活受體(NKR)的NK細胞療法,具體詳細資料尚未披露。在探索的NK042療效和安全性的AML IIT試驗中,首例輸注的急性髓系白血病(AML)患者僅發生一級CRS,無GvHD、無神經毒性。輸注后第十天,腫瘤細胞數量下降約40%。
國際藥訊
1.輝瑞RSV疫苗III期臨床積極。輝瑞雙價RSV疫苗Abrysvo用于≥60歲老人預防RSV感染導致的下呼吸道疾病(RSV-LRTD)的III期RENOIR研究(NCT05035212)長期結果積極。單次接種疫苗后,疫苗在第一個流行季和第二個流行季預防≥3種RSV-LRTD癥狀的有效率分別為88.9%和77.8%;在第二次流行季后,Abrysvo預防≥3種癥狀的RSV A以及B型的效力一致(均≥80%)。研究并未出現新的不良事件報告。
2.ARTHEx公司小核酸療法獲批IND。FDA批準ARTHEx公司靶向microRNA 23b(miR-23b)的反義寡核苷酸(AON)療法ATX-01開展I-IIa期ArthemiR™研究,評估用于治療1型強直性肌營養不良(DM1)的安全性與有效性。ATX-01與調節DM1病理發生中涉及的MBNL蛋白表達有關。目前尚無針對DM1病因的治療方法獲批。2022年12月,ATX-01已分別獲得FDA和EMA授予治療DM1的孤兒藥資格。
3.Vivani公司GLP-1植入劑臨床前研究積極。Vivani Medical公司微型、皮下GLP-1藥物植入物NPM-115(艾塞那肽)用于肥胖小鼠模型的臨床前研究結果積極。與安慰劑植入物相比,NPM-115皮下植入小鼠模型28天后體重減輕大約20%,與司美格魯肽注射治療的小鼠觀察到的體重減輕相當。臨床前研究還顯示該公司針對2型糖尿病開發的艾塞那肽植入物NPM-119單次給藥15周后,可減輕約25%的動物體重,效果持續長達六個月。
4.Pelage公司融資開發FIC脫發療法。Pelage公司完成1675萬美元A輪融資,用于推進其主打項目PP405開展Ⅱ期臨床,評估用于雄激素性脫發的治療潛力。PP405是一款創新外用制劑,旨在抑制線粒體丙酮酸載體(MPC),以重新激活休眠的毛囊干細胞。Ⅰ期臨床結果顯示,PP405(0.05%)外用治療7天,能夠顯著激活關鍵的毛囊干細胞激活標志物,并具有良好的安全性和耐受性。
5.Orbis融資加速大環藥物開發。專注于開發下一代大環藥物“nCycles”的Orbis Medicines公司宣布獲得由Novo Holdings和歐洲生命科學風險投資公司Forbion領投的2600萬歐元融資。該公司專有技術平臺nGen設計篩選的nCycles,具有口服生物可利用性和膜滲透性,有望用口服療法替代重磅生物制品,解決大環藥物設計挑戰。此外,Orbis還在開發細胞內和細胞外靶點的nCycles候選療法。
6.重癥肌無力新藥大賣12億美元。2月29日,Argenx公司發布2023年財務報表,公司全年營收12.69億美元,其中Vyvgart(艾加莫德α注射劑)和Vyvgart SC(艾加莫德α皮下注射劑)合計銷售11.91億美元。Vyvgart是一款FcRn拮抗劑,目前已在美國、歐盟和中國獲批用于AChR抗體陽性的成人全身型重癥肌無力(gMG)治療;Vyvgart SC是由Vyvgart和重組人透明質酸酶PH20(rHuPH20)共同配制。再鼎醫藥擁有艾加莫德α在大中華區的開發和商業化授權。
醫藥熱點
1.全球八分之一人口罹患肥胖癥。世衛組織科學家匯編了過去35年發表的3600多項研究的數據,以了解1990年至2022年間全球肥胖率的變化情況。研究顯示,全球有超過10億人,即每8人中就有1人罹患肥胖癥。高熱量和高糖的加工食品在世界各地越來越普遍,是肥胖率飆升的部分原因。相關論文發表于2月29日出版的最新一期《柳葉刀》雜志。
2.協和醫院成立罕見病研究院。2月29日,北京協和醫院成立罕見病診療創新發展研究院,并啟用我國首個獨立成科的罕見病醫學科專科病房,提升罕見病診治水平。罕見病診療創新發展研究院將針對臨床需求,推動“產學研用”四位一體創新發展,通過打造產品創新轉化基地、一體化診療服務平臺,建設聯合實驗室和數據支持平臺,構建罕見病診療研領域新體系。
3.華西醫院兒童心理衛生中心成立。2月28日,四川大學華西醫院兒童心理衛生中心正式揭牌成立,旨在打造構建西部地區兒童心理健康服務體系。四川大學華西醫院心理衛生中心副主任黃頤教授擔任兒童心理衛生中心主任。該中心主要收治18歲以下的各類精神疾病患者,特別針對該年齡段患者的發育特征及疾病特征,開展醫療、護理、心理、康復四位一體的綜合性、全方位的干預。
評審動態
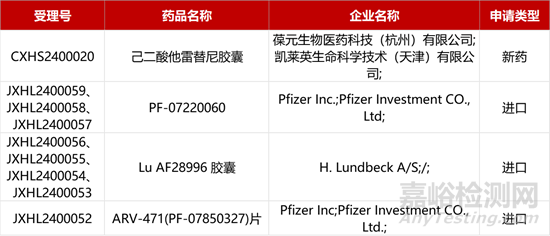
1. CDE新藥受理情況(03月04)
2. FDA新藥獲批情況(北美03月01日)






