今日頭條
靖因長效小核酸新藥國內獲批IND。靖因藥業新型siRNA療法SRSD107注射液獲國家藥監局臨床試驗默示許可,擬開發用于預防或治療動靜脈血栓。SRSD107可通過特異性肝靶向凝血因子XI(FXI)mRNA,抑制FXI的蛋白表達,阻斷內源性凝血途徑的激活,從而達到抗凝血/抗血栓的作用。目前,該新藥正在澳大利亞開展Ⅰ期臨床試驗。
國內藥訊
1.華奧泰銀屑病長效單抗啟動Ⅲ期臨床。華博生物和華奧泰生物開發的IL-17A單抗HB0017登記啟動一項Ⅲ期臨床,擬評估用于治療中重度斑塊狀銀屑病的療效和安全性。該項研究由北京大學人民醫院張建中博士牽頭開展。在Ⅰ期臨床中,HB0017(300mg)治療患者皮膚癥狀清除(PASI 90)評分均達到100%;藥物耐受性良好。此外,HB0017具有較長的半衰期,有望提供2~3月給藥1次的維持期治療方案。
2.科倫博泰ADC多項臨床將亮相AACR。科倫博泰宣布其自主開發的TROP2 ADC新藥SKB264(MK2870)將在AACR2024年會上公布用于治療晚期胃癌經治患者以及治療晚期非小細胞肺癌經治患者的兩項Ⅱ期臨床最新數據。值得一提的是,默沙東此次也將在會議上分享MK-2870針對既往治療失敗的EGFR突變或其他基因突變的非小細胞肺癌,以及聯合Keytruda一線治療PD-L1高表達非小細胞肺癌的臨床進展。
3.強生克羅恩病單抗擬納入優先審評。強生旗下古塞奇尤單抗注射液(guselkumab)獲CDE擬納入優先審評,用于治療中重度活動性克羅恩病成人患者。此前,該新藥這一適應癥已被CDE納入突破性治療品種。Guselkumab(Tremfya)是全球首個獲批的白介素23(IL-23)抑制劑,可靶向抑制IL-23這種在自身免疫性疾病中起到關鍵性作用的細胞因子。該新藥已于2019年12月在中國獲批治療銀屑病。
4.康弘1類抗腫瘤單抗獲批臨床。康弘藥業旗下康弘生物1類生物制品KH801注射液獲國家藥監局臨床許可,擬開發治療晚期實體瘤。KH801能夠與腫瘤細胞上的CD24特異性結合,通過阻斷CD24/Siglec-10“別吃我”信號,提高腫瘤相關巨噬細胞(TAM)對腫瘤細胞的吞噬作用。在動物研究中,針對CD24的治療策略對卵巢癌與三陰性乳腺癌具有治療潛力,有望為這類難治性癌癥提供新的解決方案。
5.AZ血癌ADC中國獲批臨床。阿斯利康靶向CD123抗體偶聯藥物(ADC)AZD9829獲國家藥監局臨床許可,擬開發治療CD123陽性惡性血液疾病。AZD9829能夠將TOP1i載荷遞送到表達CD123的癌細胞中,導致DNA損傷和細胞凋亡。目前,阿斯利康正在美國開展Ⅰ/Ⅱ期臨床,評估AZD9829單獨或聯合治療CD123陽性血液惡性腫瘤患者的安全性、耐受性、藥代動力學和初步抗腫瘤活性。
6.星盛新輝“合成致死”小分子獲批IND。星盛新輝小分子CHK1抑制劑XS-02膠囊獲國家藥監局臨床試驗默示許可,擬開發用于治療晚期實體瘤。抑制CHK1會觸發細胞周期阻滯,阻斷腫瘤細胞的DNA損傷應答,達到“合成致死”的效果。公布于AACR2023年會上的臨床前數據顯示,XS-02在多種實體瘤模型(尤其是PARP抑制劑原發/繼發耐藥的腫瘤PDX模型)中,顯示出良好的抗腫瘤能力,且安全性可控。
國際藥訊
1.Formosa公司改良型眼科新藥獲批上市。Formosa公司和AimMax公司開發的0.05%丙酸氯倍他索(clobetasol propionate)眼科懸液APP13007獲FDA批準上市,成為首個丙酸氯倍他索眼科產品,用于治療眼科手術后的炎癥和疼痛。在Ⅲ期臨床中,APP13007治療在清除炎癥和緩解疼痛的療效方面較安慰劑更優。遠大醫藥擁有該新藥在中國大陸、香港和澳門地區的獨家開發和商業化授權。
2.司美格魯肽慢性腎病III期臨床積極。諾和諾德公布其GLP-1激動劑司美格魯肽輔助治療合并腎功能不全2型糖尿病和慢性腎病的Ⅲ期臨床FLOW主要結果。數據顯示,與安慰劑相比,司美格魯肽使患者的腎臟疾病進展以及心血管和腎臟死亡風險降低24%,達到優效性終點。去年10月,由于司美格魯肽的療效達到預設標準,諾和諾德基于獨立數據監查委員會(DMC)的建議提前終止FLOW試驗。
3.羅氏/Alnylam長效降壓藥II期臨床成功。羅氏與Alnylam開發的RNAi療法Zilebesiran治療輕中度高血壓的II期KARDIA-2研究達到了主要終點。患者在標準治療的基礎上接受Zilebesiran(600mg,每6個月1次,皮下注射)治療,3個月后,24h平均收縮壓(SBP)較基線顯著降低;且藥物安全性良好。詳細結果將在2024年美國心臟病學會年度科學會議上公布。
4.Empros公司口服減肥復方Ⅱ期臨床積極。Empros Pharma公司口服組合配方EMP16(奧利司他/阿卡波糖)治療肥胖或超重人群的Ⅱb期臨床結果積極。數據顯示,EMP16治療使受試者平均體重減輕8%。該公司獨有配方使兩種化合物在胃腸道系統產生局部效果,增強療效的同時降低潛在的副作用。Empros計劃盡快開展兩項用于治療肥胖(伴或不伴有2型糖尿病)或超重人群的Ⅲ期臨床。
5.Exonate公司FIC眼藥水臨床積極。Exonate公司基于SRPK1抑制劑開發的眼藥水配方EXN407,在一線治療輕中度非增生性糖尿病視網膜病和輕度糖尿病性黃斑水腫患者的Ⅰb/Ⅱa期臨床中獲積極結果。EXN407通過抑制SRPK1,可選擇性地針對導致視網膜血管疾病進展的VEGF亞型,抑制眼內滲漏血管的異常生長。數據顯示,與安慰劑相比,EXN407治療能持續減少患者的黃斑厚度;有更多患者實現血管滲漏顯著減少(60%vs20%)。此外,EXN407總體耐受性良好。
6.DMD基因療法早期臨床積極。REGENXBIO公司AAV8基因療法RGX-202治療4至11歲杜氏肌營養不良(DMD)患者的Ⅰ/Ⅱ期AFFINITY DUCHENNE試驗結果積極。RGX-202旨在遞送表達微肌營養不良蛋白的轉基因進入骨骼肌和心肌組織。數據顯示,接受RGX-202劑量水平2治療的首例患者在三個月后,其微肌營養不良蛋白表達較標準對照提高75.7%,且在十周時觀察到患者血清CK水平較基線降低77%,患者的力量與運動功能獲得了初步改善。
醫藥熱點
1.王卉曉履新安徽省中醫藥管理局黨組書記。3月2日,據安徽省中醫藥管理局官網“局領導介紹”一欄信息顯示,王卉曉已任安徽省衛生健康委員會黨組成員、安徽省中醫藥管理局黨組書記。公開信息顯示,王卉曉,女,1967年11月出生,安徽合肥人,研究生學歷,中共黨員。她曾掛任安徽省合肥市廬陽區委常委、副區長;安徽省第二人民醫院黨委書記、安徽醫學高等專科學校黨委副書記等職。
2.北京積水潭醫院成立日間手術中心。3月4日,北京積水潭醫院日間手術中心正式掛牌,旨在有效減輕患者就醫負擔,推動醫院高質量發展。日間手術中心計劃開設床位15張,由手外科醫師、麻醉醫師、護理人員共同組成日間手術團隊,試運行階段主要收治手外科患者,可完成手部腱鞘炎、腱鞘囊腫、異物取出及內固定裝置取出等手外科常規手術。符合日間手術的患者可以在24小時內完成“入院、住院、出院”全流程診療。
3.湖北省這家醫院成立睡眠醫學中心。近日,隨州市中心醫院睡眠醫學中心正式成立。該中心是集睡眠障礙預防、監測、診斷與治療于一體,為患者解決各類睡眠問題的綜合診治中心。睡眠醫學中心開放病床30張,設置于季梁院區心身醫學科內,配備多導睡眠監測系統(PSG)、重復經顱磁刺激治療儀、團體生物反饋治療儀、失眠治療儀、心理CT等先進設備,并設有睡眠監測室、心理測量室、物理治療室、個體心理治療及團體心理治療室。
評審動態
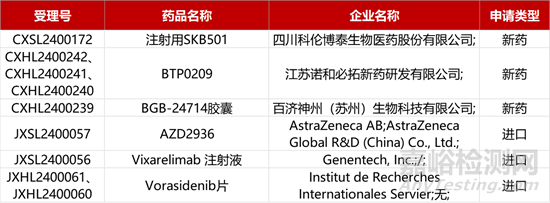
1. CDE新藥受理情況(03月06)