近期,賓夕法尼亞州立大學程寰宇﹑楊健教授和電子科技大學林媛教授在科愛出版創辦的期刊 Bioactive Materials 上聯合發表綜述文章:用于傷口愈合與治療智能敷料的最新進展。傷口實時監測與治療是傷口愈合的關鍵,這推動著傷口敷料往智能化和多功能化方向發展。該文詳細總結了閉環智能傷口敷料的材料設計﹑結構設計與實時監測單元的最新研究進展,并指出可延展傳感器以及無線通訊技術在傷口監測與藥物管理的重要作用以及智能傷口敷料的傳感治療多功能集成的設計與加工上挑戰。
1、研究內容簡介
術后傷口恢復和免疫缺陷造成的慢性傷口潰爛是臨床醫學上的難點,且患者比例逐年上升。通過使用傷口敷料固定傷口切面﹑抵抗細菌感染﹑施加生長因子﹑誘導免疫系統有序反應是加速傷口愈合的主要手段。傳統的傷口敷料研究關注敷料本身的機械性能,包括黏性和內聚力,自然界中廣泛存在的生物黏附現象從材料和結構兩方面為傷口敷料設計提供了極大靈感。近期提出的水凝膠由于其良好的生物兼容性﹑優異的藥物輸運性以及外場可控交聯方式,在傷口敷料方向展現了巨大的應用前景。最新研究表明光﹑電﹑機械刺激和它們之間的協同刺激都可以促進生長因子分泌和組織再生,極大地加快傷口愈合。除了傷口治療,將柔性傳感器集成在敷料中對傷口進行實時檢測和評估也是閉環智能傷口敷料的重要功能。傷口傳感數據通過先進的無線技術與終端設備進行交互,促發藥物管理系統進行智能化藥物釋放,保證傷口有效愈合。該文章從材料﹑結構以及系統三個方面介紹了敷料,傳感器以及無線技術在閉環智能傷口敷料的最新研究進展進行了詳細綜述 (圖1)。
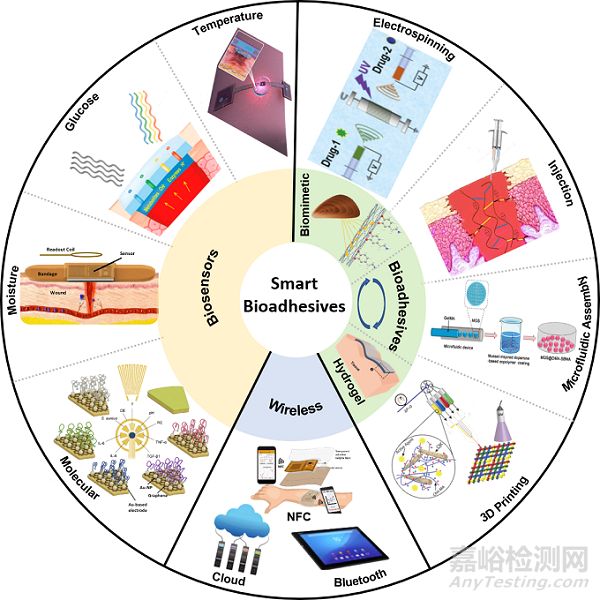
圖1:智能傷口敷料技術總結
一、免疫調節水凝膠敷料
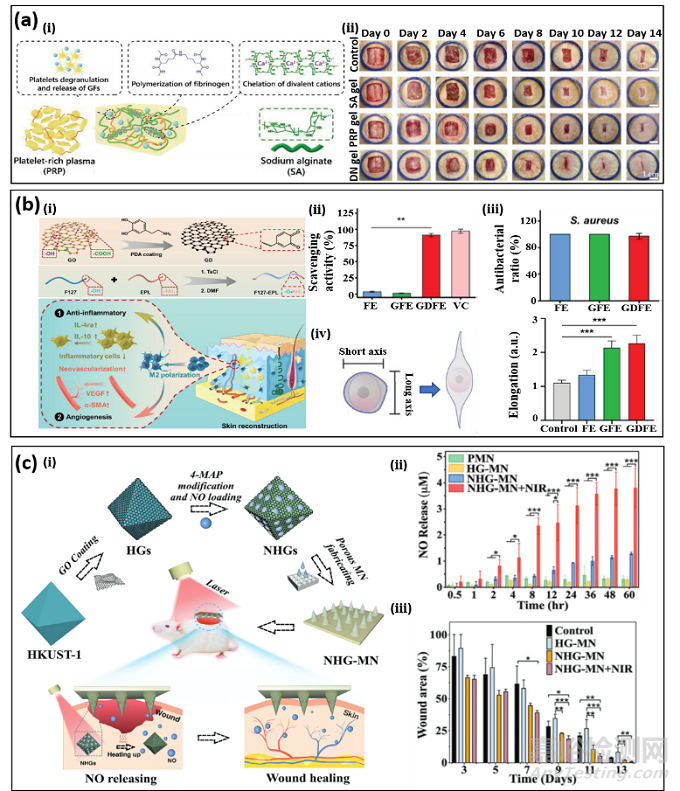
傷口愈合是一個有序的先天性與特異性免疫反應參與過程,包含了凝血﹑炎癥﹑修復與成熟四個階段。先天性免疫系統在炎癥期檢測到異體信號,然后特異性免疫系統開始清理病原體。參與免疫反應的細胞與組織之間的協同工作依靠一套可靠的信號系統,包括生長因子﹑細胞因子﹑趨化因子等。信號交流紊亂會引起免疫反應失效,從而導致傷口無法愈合,甚至是截肢或者死亡。例如,傷口愈合過程中細胞因子和活性氧的過度表達會導致促炎性到促再生階段過渡的延時,導致傷口潰爛。考慮到傷口愈合是一個復雜生理過程,相比于直接藥物管理,通過特定的物理化學刺激促發人體自身免疫反應是治療傷口感染或發炎更有效的方式(圖2)。水凝膠因為其可控的化學組分﹑機械性能﹑交聯促發機制﹑藥物加載和釋放方式,是一種優良的傷口敷料。前期研究發現,一些特定水凝膠本身化學成分具有免疫調節功能,比如玻尿酸和殼聚糖水凝膠。另外,通過對水凝膠進行表面修飾或者摻雜也可以達到免疫調節的作用。例如,對F127水凝膠摻雜多巴胺修飾氧化石墨烯和ε-聚賴氨酸可以同時取得抗菌和免疫調節的作用。該水凝膠可以通過多巴胺到多巴醌的氧化反應有效降低氧化自由基的濃度,進而促進巨噬細胞向M2表型細胞極化,加速糖尿病患者傷口愈合。一種基于血漿含有多種生物活性分子,具有天然的免疫調節功能。通過在血漿中引入海藻酸鈉形成雙網絡水凝膠結構,可以有效解決血漿機械強度低和生物活性因子釋放過快等問題,從而加速傷口愈合。一氧化氮是重要的神經遞質和免疫反應的生物信號分子,在傷口由發炎過渡到修復階段擔當著重要作用,如何在傷口處持續地釋放一氧化氮氣體成為了研究的難點問題。多孔的MOF顆粒是優良的一氧化氮氣體載體,通過對顆粒外表面行進氧化石墨烯修飾然后加載在聚乙二醇水凝膠的交聯網絡中,可以實現紅外光控制的一氧化氮可持續釋放,進而調節免疫系統加快傷口愈合。
圖2:免疫調節水凝膠. (a)基于血漿與海藻酸鈉雙網絡水凝膠;(b)F127水凝膠摻雜多巴胺修飾氧化石墨烯和ε-聚賴氨酸同時具有抗菌和免疫調節的作用;(c)MOF顆粒修飾聚乙二醇水凝通過可持續釋放一氧化氮氣體調節傷口愈合免疫反應
二、柔性生物傳感器
慢性傷口恢復是一個動態且漫長的過程,患者需要經常去醫院做傷口診斷和治療,比如清理傷口和更換敷料,而且傷口評估主要依靠醫生的經驗和主觀判斷,往往導致錯誤判斷。通過柔性生物傳感器對傷口狀態進行科學的﹑實時的診斷和評估已經成為了傷口管理的新趨勢,其中監測指標包括pH值﹑溫度﹑濕度﹑尿酸﹑葡萄糖與氧氣濃度等。pH值主要影響炎癥反應﹑膠原蛋白形成與血管再生等過程。對于急性傷口,pH值在4到6之間,可以有效阻止細菌增殖。由于免疫系統紊亂,慢性傷口的pH值在7到9之間波動,很容易導致細菌入侵和傷口感染。溫度對參與傷口愈合過程的各種酶的反應活性,傷口局部血流和淋巴細胞遷移具有重要影響,因為被認為是傷口愈合過程中最具參考意義。研究表明,傷口溫度低于33 °C會降低纖維母細胞﹑中性粒細胞以及上皮細胞的活性,不利于傷口愈合。人體無法分泌尿酸代謝酶,而某些細菌可以直接進行尿酸代謝,因為傷口滲出物較低的尿酸含量可能預示著傷口感染。較高的葡萄糖濃度會阻礙毛細血管的新生,進而導致組織壞死。傷口處充足的氧氣濃度可以刺激白細胞進入傷口區域﹑抵抗細菌感染﹑加快局部新陳代謝,促進組織再生。
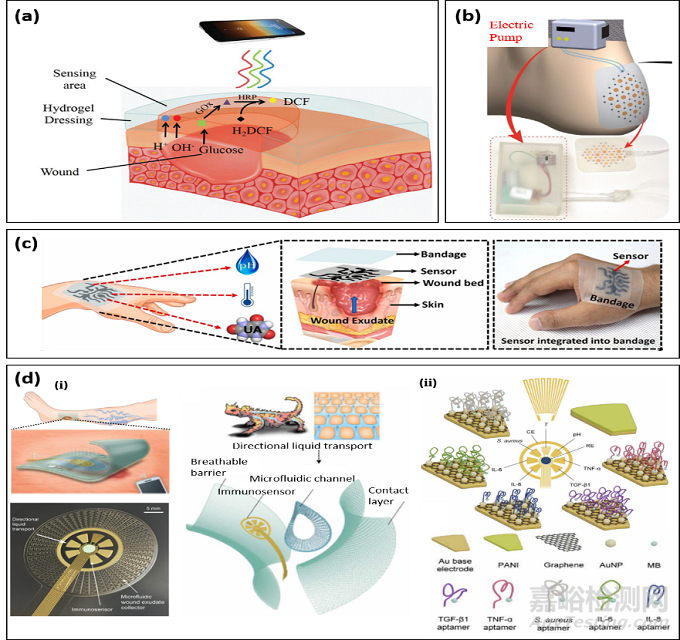
針對這些關鍵傷口指標,一系列新穎的多功能柔性傳感器被提出并且在展現出巨大的應用前景(圖3)。基于酸堿指示劑和熒光效應,一種多功能水凝膠可以同時監測傷口處pH和葡萄糖濃度值。一種紙基微流管道的貼片可以通過微流泵往傷口處定向輸送氧氣,有效提高氧氣濃度高達25-50%,加快傷口愈合速度;基于熒光效應,釕化合物可以準確檢測5-26 ppm的氧氣濃度范圍。納米材料具有優異的電化學性能,被廣泛應用生物傳感。基于激光誘導石墨烯和MXene的復合材料可以同時檢測傷口處的pH值和尿酸濃度,并且線性度高達0.99。此外,該復合材料的電阻溫度系數在25-50 °C范圍內為0.09% ?C-1并具有很高的線性溫度響應性能(~0.99)。最近,一種專門針對慢性傷口檢測的智能貼引起了學界的關注,它集成了微流控芯片﹑免疫炎癥因子(包含tumor necrosis factor–α (TNF-α), interleukin-6 (IL-6), IL-8, transforming growth factor–β1)﹑細菌﹑溫度傳感以及無線傳輸模塊。受鯊魚牙齒的啟發,該微流通道可以有效地收集微量傷口滲出液并將其輸運到檢測區域。通過對電化學傳感器工作電極進行金納米顆粒與石墨烯修飾,接著引入適配體,炎癥因子以及細菌濃度通過方波伏安法標定和測量。
圖3:用于傷口監測的柔性生物傳感器. (a)基于酸堿指示劑和熒光反應監測傷口pH值與葡萄糖濃度;(b)釕化合物的熒光反應檢測傷口處氧含量;(c)基于激光誘導石墨烯和MXene復合材料的柔性pH,溫度與尿酸傳感器;(d)針對慢性傷口炎癥檢測的適配體電化學傳感器
三、多功能或閉環傷口敷料
集成診斷和治療功能的智能傷口敷料具有廣闊的應用前景。通過柔性傳感器實時、原位地監測傷口生理指標并及時釋放藥物可以大大降低置換敷料帶來的痛苦,減少傷口感染和發炎的風險(圖4)。用氨基苯硼酸(ABA)嫁接金納米顆粒修飾的纖維素敷料不僅具有優良的抗菌性,而且可以根據熒光強度判斷敷料上納米藥物殘余,從而及時進行敷料更換。由于傷口滲出物及其微量,對它進行有效的收集是準確檢測傷口狀況的關鍵,利用特殊結構設計的微流管道是解決這一難題的有效途徑。由于毛細力的作用,傷口滲出液會自發地被收集到光子晶體檢測區域,乳酸和鈣防衛蛋白等傷口標記分子可以通過熒光反應進行標定。當相關指標異常時,加載在多孔微針的生長因子會主動釋放,從而加快傷口愈合。另一方面,無線技術可以極大地減小智能傷口敷料的尺寸和增加其功能多樣性,包括非接觸式檢測﹑遠程監控與藥物管理。例如,導電纖維作為傷口縫線與插值電極構成LC振蕩電路,可以通過共振頻率的偏移和幅值變化來遠程監測內部傷口泄露與縫線斷裂。集成溫度傳感器﹑LED﹑藥物加載水凝膠以及近場耦合通信的智能閉環傷口敷料可以實時監測傷口溫度﹑評估傷口感染程度﹑傳輸傳感數據﹑接收遠程藥物管理命令。實時傳感數據與藥物管理命令的通過近場傳輸相互交互可以有效的避免治療不及時和藥物亂用帶來的嚴重后果。基于藍牙無線傳輸的智能水凝膠傷口敷料具有更遠的工作距離,傷口處的異常溫度上升觸發UV-LED開啟,抑制細菌生長。
圖4:集成生物檢測、治療與無線數據傳輸的智能傷口敷料。(a)基于金納米顆粒藥物的抗菌傷口敷料及其納米藥物殘留自檢測機制;(b)集成微流管道和多孔水凝膠微針進行有效傷口滲出液收集與生長因子釋放;(c)導電纖維傷口縫線與插指電極構成的LC震蕩電路對內部傷口泄露與縫線斷裂進行監測;(d)基于無線近場傳輸的閉環智能傷口敷料實現傷口溫度﹑pH﹑尿酸的檢測以及抗菌藥物的釋放;(e)基于藍牙無線傳輸的閉環智能傷口敷料實時監測傷口溫度異常并遠程開啟UV-LED進行殺菌