您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2025-03-13 08:36
摘要
目的 通過闡述凍干注射劑輔料選擇的基本考慮,為藥學開發提供借鑒和思考。方法 匯總了近年來 FDA 已上市化藥凍干注射劑的輔料使用情況,包括輔料組成、FDA 收載的最大輔料用量等,論述凍干注射劑輔料選擇需重點考慮的問題。結果 已上市凍干注射劑中有四分之一不使用輔料,而使用最多的輔料類別分別是凍干賦形劑、緩沖鹽和 pH 調節劑,其他輔料包括增加溶解的輔料、抗氧劑等。結論 凍干注射劑輔料的選擇要重點考慮安全性、處方合理性、功能性指標及輔料控制方面的問題。
【關鍵詞】 凍干注射劑; 輔料; 安全性; 處方合理性; 功能性指標
凍干注射劑是指采用冷凍干燥法制備的用于注射給藥的制劑。凍干工藝適合于熱不穩定原料藥,有些原料藥因自身溶解性、劑量以及凍干成型性問題,需使用輔料以改善凍干產品的功能特性和穩定性。
1.已上市凍干注射劑輔料使用情況匯總
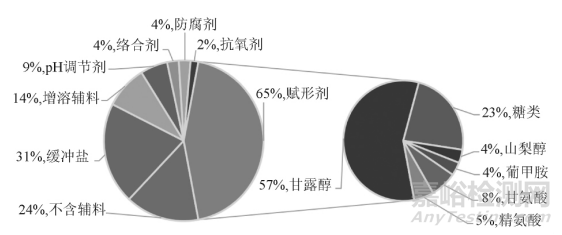
從 2009 年至 2019 年( 統計截止至7月) ,美國食品藥品監督管理局( Food and Drug Administration,FDA) 上市批準新藥 385 款,其中新分子實體新藥280 款,化藥凍干注射劑共有 23 種,見表 1。Baheti等[1]于 2010 年發表文章匯總了 2009 年之前 58 種美國已上市化藥凍干注射劑的信息,見表 2。對美國已上市凍干注射劑的處方進行匯總分析,發現約24% 的制劑不添加任何輔料。使用輔料的制劑中,約 65% 的制劑使用凍干賦形劑,凍干賦形劑包括以甘露醇為代表的多元醇類、低分子糖類、少量的氨基酸類以及部分聚合物類; 緩沖鹽在凍干注射劑中的使用占比約 31% ,主要包括枸櫞酸、酒石酸、磷酸、琥珀酸及其鹽類等; 此外凍干制劑中還包括增加溶解度的輔料( 羥丙基-β-環糊精、聚山梨酯 80 等) 、pH 調節劑( 氫氧化鈉、鹽酸) 、絡合劑[乙二胺四乙酸( EDTA) 及鹽等]、防腐劑( 苯甲醇和羥苯甲酯) 以及抗氧劑( 生育酚) 等輔料。FDA 已上市凍干注射劑中各類輔料在制劑中的使用比例見圖 1。
▲表 1-2009 年至 2019 年 7 月 FDA 上市化藥類凍干注射劑
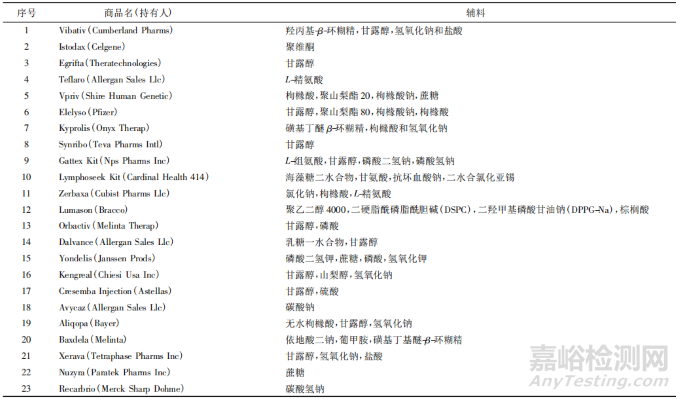
▲表 2-2009 年前 USA 已上市化藥凍干注射劑
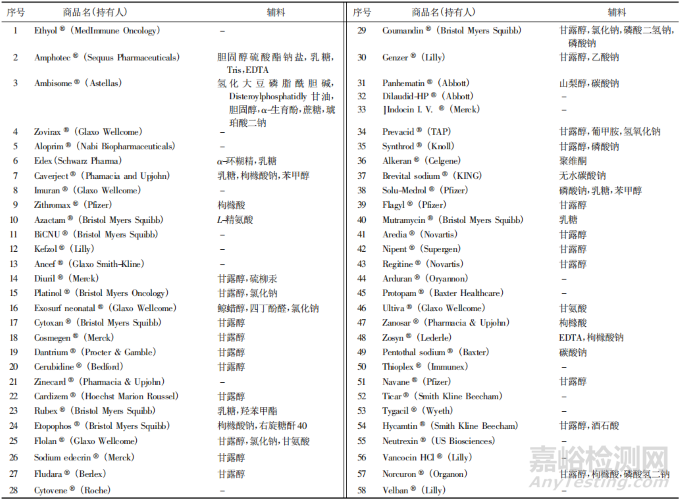
▲圖1-已上市凍干注射劑中輔料的使用情況
2.常用輔料的用量情況
FDA IID( Inactive Ingredient Database) 收載了不同給藥途徑下輔料單劑量最大用量,其中注射劑中常用各類輔料的用量及用藥途徑信息匯總見表 3。數據庫中不同劑型的計量單位不同,凍干注射劑輔料單劑量最大用量以 3 種方式表述,即% w /v( 凍干粉末輔料用量通常以復溶后產品中輔料的百分比) 、% ( 重量百分比) 或者 mg( 重量) 表示[2]。IID數據庫僅提供單劑量制劑輔料的最大用量,每日給藥劑量、用藥周期、用藥人群信息均未提供,因此無法推斷輔料每日最大用量情況。盡管如此,IID收載數據仍可為輔料用量確定提供支持性依據。
▲表3-FDA IID 收載凍干注射劑常用輔料注射途徑最大用量情況
3.凍干注射劑中的輔料類別
《美國藥典》按功能將輔料分為 45 類,其中與凍干注射劑相關的輔料包括 Buffering Agent( 緩沖鹽) 、Bulking Agent for Freeze-Drying( 凍干賦形劑) 、Complexing Agent( 絡合劑) 、Tonicity Agent( 滲透壓調節劑) 、Wetting and /or Solubilizing Agent( 潤濕和/或增溶劑) 等。對凍干注射劑常用輔料類型簡單介紹如下。
3. 1 凍干賦形劑
凍干賦形劑主要起到支持凍干藥餅結構的作用。良好的藥餅結構能夠保證凍干過程中溶劑順利逸出,藥餅結構坍塌會增加溶劑揮發阻力,導致局部溶劑殘留增加。如果溶劑為水,那么局部水分過高可能會導致活性藥物成分的降解。一些總固體含量小于 2%的小規格藥物凍干過程需要凍干賦形劑支撐[3]。原料藥凍干成形性良好,大規格制劑不需要輔料即可凍干。甘露醇是化藥凍干注射劑中最常用的賦形劑,其他常用賦形劑依次為糖類( 如乳糖、蔗糖) 、氨基酸類( 如甘氨酸、精氨酸) 和聚合物類( 如聚維酮和聚乙二醇) 等。凍干賦形劑可能為結晶型或非結晶型。甘露醇常見為結晶型,包括 α,β 和 δ3 種晶型[4],但當甘露醇形成過飽和溶液時,也會形成無定形態[5-6]。非結晶型凍干賦形劑主要包括糖類和氨基酸類,例如海藻糖、乳糖、精氨酸、甘氨酸、賴氨酸等[7]。
3. 2 緩沖鹽
添加緩沖鹽的目的是為了控制藥液的 pH 值,常用的緩沖鹽包括枸櫞酸、酒石酸、磷酸及其鹽等。對 pH 敏感藥物控制溶液 pH 可防止藥物在配液、復溶和儲存過程中降解。緩沖鹽選擇需要慎重,比如磷酸鈉在冷凍過程中可能會結晶析出,pH 發生偏移[8]。緩沖鹽用量的確定不完全取決于藥物在溶液中最穩定的 pH 條 件,有時候在溶液中穩定的pH,在凍干制劑中不一定最穩定。如 莫 西 普 利( moexipril) 在水溶液和凍干制劑中 pH 分別為 2 和8 左右水解程度最低,磺胺在 pH 3. 4 ~ 6. 0 條件下凍干粉的酸化程度始終高于溶液[9-10]。
3. 3 增加藥物溶解度的輔料
這類輔料的主要作用是增加原料藥的溶解度,根據發揮增溶作用機制分為表面活性劑、有機共溶劑和包合物等。表面活性劑通過形成膠束增加水不溶性藥物的溶解度。注射劑常用的表面活性劑是聚山梨酯 80,其凍干的玻璃化轉變溫度低,因此不建議大量添加。可以將表面活性劑加入專用溶劑中用于凍干粉的復溶,以避免對凍干過程的影響,如聚山梨酯 80 濃度增加也會增加甘露醇 δ 晶 型 的 比例[11]。增加藥物溶解度的另一個方法是采用水和有機溶劑的共溶劑。與水相比,有機溶劑共溶劑可以加快藥物的溶解,且低沸點有機溶劑可以提高凍干效率,還可以增強溶液的無菌保證水平[12]。使用共溶劑時可能需要特殊的工藝步驟和設備,并需要對制劑中殘留溶劑進行控制。最常用的共溶劑是叔丁醇-水組合,在冷凍過程中過飽和度和成核度增加,結晶速率更快[13]。另外,也可以采用其他增溶劑來增加藥物溶解度,最常見的是環糊精類輔料。環糊精類將適當大小的藥物分子包裹在空穴內部,可以增加水溶性差藥物的溶解性[14]。經過改性修飾的環糊精具有更好的水溶性,如羥丙基-β-環糊精作為增溶劑已經用于注射途徑給藥[15]。
以上輔料類型是化藥凍干注射劑中較為常見的三類輔料,其他類型的輔料還包括 pH 調節劑、抗氧劑、絡合劑、防腐劑等,根據制劑本身特性及臨床使用要求選擇。
4.輔料選擇的考慮
結合實際工作中遇到的一些共性問題,凍干注射劑輔料選擇需要重點關注以下方面。
4. 1 安全性
凍干注射劑中的輔料必須符合注射用要求,在滿足制劑需要的前提下,輔料的種類及用量應盡可能少,并且應盡可能采用注射劑常用輔料。FDA IID數據庫和國家監局藥品審評輔料數據庫,可以查閱常用凍干注射劑的輔料使用情況,如最大用量、使用途徑等。對于已有注射使用歷史的輔料,若擬定輔料用量可能超出相應給藥途徑的歷史最大使用量,應提供相關安全性數據等資料[16]。
目前《中國藥典》中收載的注射用輔料非常有限。評估輔料是否滿足注射要求,首先關注所選輔料在注射途徑的使用經驗和歷史( 包括輔料種類和用量) 。其次,應對微生物負荷和內毒素進行適當控制。最后,還需要考慮輔料用于注射途徑是否存在其他安全性風險,如過敏性問題、與其他藥物在體內相互作用問題等。申請人需要結合適應證、用法用量、用藥周期等,從臨床風險獲益比的角度全面評價該輔料的安全性,并應采取適當的措施降低由輔料引入的安全性風險。
以聚維酮( povidone,PVP) 為例,從安全性角度分析其用于注射劑的考慮。PVP 是 N-乙烯基酰胺類聚合物,早期靜脈注射 PVP 可用作代血漿。不同相對分子質量 PVP 靜脈注射后,其在體內的蓄積情況也不相同,蓄積的主要風險是影響凝血功能。相對分子質量在 110 000 ~120 000 之間,PVP 在體內會蓄積很長時間,低于 40 000 相對分子質量的 PVP 幾天內清除完全,用于代血漿的 PVP 相對分子質量一般在25 000 ~40 000[17]。FDA 于 1978 年頒布聯邦公報( 43Federal Register,第 14 743 頁) 對申請上市用于休克用代血漿的 PVP 注射液實行撤市,并且聲明任何與該產品相關或者類似的用于靜脈注射的產品都不批準。撤市的 PVP 注射液是一種含 3. 5% PVP 的生理鹽水注射液[18]。3. 5% PVP 注射液作為代血漿大量靜脈注射存在較大的安全風險,這可能與 PVP 用量以及 PVP 型號( 相對分子質量) 密切相關。但不能一概而論認為所有 PVP 均不能用于注射給藥,應結合產品適應證、給藥途徑、PVP 型號以及用量綜合評估。目前 FDA 批準的 ISTODAX 圖片和 ALKERAN 圖片及其仿制制劑均使用了 PVP K12 作為凍干賦形劑,ISTODAX 用于治療外周 T 細胞淋巴瘤,ALKERAN 用于治療多發性骨髓瘤。FDA IID 數據庫收載 PVP 注射途徑其安全用量最大劑量為每支 20 mg 或者 0. 5%。
另外一個輔料安全性的例子就是聚山梨酯 80。聚山梨酯 80 具有增加藥物進入大腦的潛在作用,如使用聚山梨酯 80 作為輔料需關注主藥通過血腦屏障的風險。其次,聚山梨酯 80 在靜脈給藥后可能發生過敏性休克,過敏患者應避免使用含聚山梨酯 80的藥物。此外,聚山梨酯 80 靜脈給藥后出現心血管方面副作用,這可能與輸注速率相關,可采用較慢輸注速度來降低風險[19]。
4. 2 處方的合理性
一方面,關注輔料對產品質量的影響。通過原輔料相容性研究確定處方中各輔料用量、配比的合理性,同時關注穩定性放置期間出現的質量變化,如結構坍塌、復溶時間延長以及雜質超限等,進而從處方設計、工藝控制、包材相容性等方面進行分析,確定影響產品質量的原因并加以控制。例如,甲強龍琥珀酸鈉采用甘露醇作為凍干賦形劑藥物水解率高于乳糖,原因可能是甘露醇和乳糖凍干后藥餅微環境內含水量不同[20]。另一方面,應關注輔料對產品工藝過程及凍干程序的影響。凍干制劑中輔料種類及比例不同,共晶熔化溫度( Teu ) 或玻璃態轉變溫度( Tg ) 也有所不同,則凍干程序溫度和時間不同。預凍溫度需保持在 Teu或 Tg以下,干燥溫度不宜高于Teu或 Tg,以避免引起藥餅結構坍塌[21-22]。但也有研究表明,干燥溫度適當高于 Tg也不會引起藥餅宏觀結構的坍塌[23]。
對于仿制凍干注射劑,需要保證與原研制劑處方的 Q1 /Q2 一致,部分 pH 調節劑、抗氧劑以及抑菌劑如與原研不同,應闡述與原研不同的理由,并研究證明輔料變化不影響產品的安全性和有效性[24]。
4. 3 功能性指標
功能性指標用于評價輔料在制劑中的功能。例如,晶型是賦形劑最重要的功能性指標,易于結晶的賦形劑有助于保持初級干燥過程中形成的藥餅結構完整性,從而防止藥餅結構塌陷,無定型的賦形劑達到一定濃度,也能夠防止結構坍塌。賦形劑的水分保留和吸附能力也是其重要的功能性指標,水分殘留高低影響制劑的穩定性。也有研究表明,不同賦形劑的哈密特酸度( Hammett acidity) 不同,導致藥物降解程度不同[25]。
4. 4 輔料控制方面
要掌握影響制劑性能的關鍵輔料生產工藝和質量控制情況。對于關鍵輔料,建議評估不同批次及不同生產商輔料對制劑質量及生產工藝的影響,根據自身開發藥品的特性制定合理的內控標準,特別是功能性指標,必要時需要在申報資料中明確輔料的商品名和商業級別。
5.展 望
用于注射途徑的輔料,其安全性是首先要考慮的,其次是處方中輔料使用的合理性以及輔料功能性指標的考察。最后,對關鍵輔料應制定適當的內控標準。建議凍干注射劑處方開發,應該從單獨的原料藥開始,根據原料藥特性以及工藝需要逐漸增加輔料的使用。在處方開發過程中不斷積累數據,為后續產品的放大及工藝變更提供了充足的知識支撐。現在原輔料實行備案登記制度,申請人應當根據自身制劑的特點,合理控制并選擇輔料。
參考文獻
[1] BAHETI A,KUMAR L,BANSAL A K. Excipients used in lyophilization of small molecules[J]. J Excip Food Chem,2016,1( 1) : 1135.
[2] FDA. Using the Inactive Ingredient Database Guidance for Industry. [EB /OL]. [2019-07]. https: / /www. fda. gov /regulatory information /search-fda-guidance-documents/using-inactive-ingre dient-database-guidance-industry.
[3] JENNINGS T A. Effect of formulation on lyophilization,part 1[J]. IVD Technol Mag,1997,3( 2) : 42-49.
[4] FRANKS F,AUFFRET T. Freeze-Drying of Pharmaceuticals and Biopharmaceuticals[M]. Cambridge: RSC Publishing,2007.
[5] SEARLES J A. Freezing and annealing phenomena in lyophilization,in: L. Rey,J. C. May ( Eds. ) ,Freeze-Drying /Lyophilization of Pharmaceutical and Biological Products[M]. NewYork: Marcel Dekker,Inc. ,2004.
[6] JENNINGS T. The importance of process water,in: Lyophilization,Introduction and Basic Principles[M]. Englewood: Interpharm Press,1999.
[7] PATEL S M,PANSARE S K. Optimized ratios of amino acidsand sugars as amorphous stabilizing compounds in pharmaceuticalcompositions containing high concentrations of protein-based therapeutic agents,2017.
[8] GOMEZ G,PIKAL M J,RODRIGUEZ-HORNEDO N. Effect of initial buffer composition on pH changes during far-fromequilibri um freezing of sodium phosphate buffer solutions[J]. PharmRes,2001,18( 1) : 90-97.
[9] STRICKLEY R G,VISOR G C,LIN L H,et al. An unexpectedpH effect on the stability of moexipril lyophilized powder[J].Pharm Res,1989,36( 6) : 971-975.
[10] RAMPRAKASH G,KOUSTUV C,LARRY G,et al. Impactof freeze-drying on ionization of sulfonephthalein probe molecules in trehalose-citrate systems[J]. J Pharm Sci,2010,95( 7) : 1498-1510 .
[11] HAIKALA R,EEROLA R,TANNINEN V P,et al. Polymorphicchanges of mannitol during freeze-drying: effect of surface-activeagents[J]. PDA J Pharm Sci Technol,1997,51( 2) : 96-101.
[12] GOVINDARAJAN R,CHATTERJEE K,GATLIN L,et al. Impact of freeze-drying on ionization of sulfonephthalein probe molecules in trehalose-citrate systems[J]. J Pharm Sci,2006,95( 7) : 1498-1510.
[13] TELANG C,SURYANARAYANAN R. Crystallization of cephalothin sodium during lyophilization from tert-butyl alcohol-watercosolvent system[J]. Pharm Res,2005,22( 1) : 153-160.
[14] LOFTSSON T,BREWSTER M E. Pharmaceutical applications ofcyclodextrins. 1. Drug solubilization and stabilization [J]. JPharm Sci,1996,85( 10) : 1017-1025.
[15] GOULD S,SCOTT R C. 2-Hydroxypropyl-beta-cyclodextrin( HP
beta-CD) : atox-icologyreview[J]. Food Chem Toxicol,2005,43( 10) : 1451-1459.
[16] National Medical Products Administration. Announcement on FurtherImproving Related Issues Concerning Drug Review and Approval andSupervision Work ( Draft for Comment) [EB/OL]. [2017-12-22].
http: / /www. nmpa. gov. cn /WS04 /CL2101 /336058. html.
[17] RAVIN H A,SELIGMAN A M,FINE J. Polyvinyl pyrrolidone as a
plasma expander[J]. New Engl J Med,1952,247( 24) : 921-929.
[18]FEDERAL REGISTER,VOL. 43,NO. 68-FRIDAY,APRIL 7,
1978. [EB/OL]. [2018-11-19]. https: / /s3. amazonaws. com/ar
chives. federalregister. gov /issue _ slice /1978 /4 /7/14742-14744. pdf #
page =2.
[19] European Medicines Agency. Guideline,Information for the packageleaflet regarding polysorbates used as excipients in medicinal prod
ucts for human use. [EB/OL]. [2018-11-19] .https: / /www. ema. europa. eu /en /documents/scientific-guideline /draft-information-package-leaflet-regarding-polysorbates-used-excipients-medicinal-products-human_en. pdf.
[20] HERMAN B D,SINCLAIR B D,MILTON N,et al. The effect ofbul
king agent on the solid-state stability of freeze dried methylprednisolone
sodium succinate[J]. Pharm Res,1994,11( 10) : 1467-1473.
[21] SERIGO A,RAMBHATLA S,PIKAL M J. Heat and mass transfer
scale-up issues during freeze drying,I: atypical radiation and the
edge vial effect[J]. AAPS Pharm Sci Tech,2003,4( 2) : 114-127.
[22] LAM T,STRICKLY R G,VISOR G C. An unexpected pH effect
on stability of moexipril lyophilized powder[J]. Pharm Res,2004,6( 11) : 971-975.
[23] KASPER J C,WINTER G,FRIESS W. Recent advances and fur
ther challenges in lyophilization[J]. Eur J Pharm Biopharm,2013,
85( 2) : 162-169.
[24] The Drug Evaluation Center of National Medical Products Adminis
tration. Notice on Publicly Soliciting Opinions on Technical Require
ments for Consistency Evaluation of Listed Chemical Generic Drugs
( Injections) [EB/OL]. [2017-12-22]. http: / /www. cde. org. cn/
news. do? method = viewInfoCommon&id =314268.
[25] LU E,EWING S,GATLIN L,et al. The effect of bulking agents
on the chemical stability of acid-sensitive compounds in freeze
dried formulations: sucrose inversion study[J]. J Pharm Sci,
2009,98( 9) : 3387-3396.

來源:中國藥學雜志


