您當前的位置:檢測資訊 > 監管召回
嘉峪檢測網 2025-03-19 11:02
FDA發布關于美敦力明星產品---Pipeline Vantage系列栓塞器械一級召回。
召回范圍
立即停用并召回所有Pipeline Vantage 027型號器械;
更新Pipeline Vantage 021型號器械的使用說明。
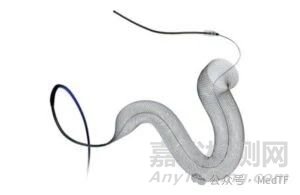
器械用途
美敦力采用屏蔽技術(Shield Technology)的Pipeline Vantage栓塞器械用于治療腦動脈瘤。該血管內介入器械通過微創導管植入血管,將編織管輸送至動脈瘤位置以阻斷血流。
召回原因
使用相關器械時及術后,其柔性編織管部分貼附血管壁失敗或無法維持貼附(貼壁不全和/或編織體變形)的報告顯著增加;
可能出現的風險包括:貼壁不全、編織體變形(亦稱“魚嘴樣變形”)、編織體狹窄或塌陷;
女性(尤其45歲以下)風險更高;
使用受影響器械可能導致嚴重健康后果,包括血栓、卒中或死亡。
造成后果
Pipeline Vantage 027型號:報告13例傷害事件及4例死亡。
Pipeline Vantage 021型號:報告4例傷害事件,無死亡案例。
美敦力解決措施
立即停用027型號器械并退回所有未使用庫存;
使用021型號器械前務必閱讀更新版操作說明;
更新版說明旨在優化器械尺寸選擇及支架編織體釋放技術,以降低風險。

來源:MedTF


