您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2025-03-13 16:48
為避免制粒生產過程中粉塵的飛揚對生產環境造成污染,本研究對一步制粒密閉生產技術進行了探討。采用 L8(27) 進行正交試驗,以顆粒粒度、顆粒水分等為考察指標,優選感冒清熱一步制粒工藝。結果確定了最佳的一步制粒工藝參數:風機頻率在 20 ~ 60 Hz 之間,物料溫度維持在 60-80 ℃(并根據物料溫度調節風機頻率),濾袋抖動時間設為 60 s,濾袋抖動間隔時間為 10 s,濃縮液密度為 1.1,輔料與濃縮液的比例為 2:1,進風溫度為 70 ℃,噴液流量為 1.0 L/min,霧化壓力為 0.2 MPa,干燥時間為 10 min。中試驗證表明,顆粒的性狀、粒度、水分、溶化性,顆粒鑒別檢查以及葛根素含量等各項指標均符合質量標準。結論是一步制粒在中藥浸膏和輔料的應用中,提高了生產效率,降低了勞動強度,并有效避免了傳統濕法制粒過程中多步驟、間歇式生產導致的粉塵飛揚問題,對生產環境造成的污染。感冒清熱一步制粒工藝具有良好的重現性,為一步制粒密閉技術的應用提供了參考依據。
感冒清熱顆粒為常用臨床用藥,能夠疏風散寒,解表清熱。該藥物適用于治療風寒感冒引起的頭痛發熱,惡寒身痛,鼻流清涕以及咳嗽咽干等癥狀 [1]。為了應對濕法制粒間歇式生產中人工操作的復雜性 [2-4],并減少多步驟生產過程中粉塵飛揚對生產環境的污染,企業利用一步制粒技術,將物料混合、噴加粘合劑、干燥等操作步驟連續進行,以實現制粒過程的密閉生產,這種方法具有顯著的優勢 [5-8]。基于此,企業采用一步制粒頂噴工藝技術,對感冒清熱一步制粒進行了中試工藝研究。
1.實驗材料
1.1 實驗設備
使用 TDH-500 多功能提取濃縮罐、LGL-30 流化床制粒干燥機。
1.2 檢驗儀器
MB23 水分分析儀、U3000 高效液相色譜儀、WGH-30 雙光束紅外分光光度計等。
1.3 物料
中藥材:荊芥穗、薄荷、防風等。
輔料:蔗糖、糊精等
2.方法與結果
2.1 濃縮液制備
將處方量的薄荷、荊芥穗、紫蘇葉三味藥材加入 10 倍量的蒸餾水以收集揮發油,密閉保存備用。水溶液通過100 目濾網過濾后備用。藥渣與防風、柴胡、葛根等八味藥材進行 2 次提取,第一次加水 10 倍量,提取 2 h ;第二次加水 8 倍量,1 h。提取液通過 100 目濾網過濾,合并兩次提取液與水溶液,并減壓濃縮至所需密度備用。
2.2 確定因素和水平
按一步制粒頂噴技術參數和操作程序進行操作,設定風機頻率為20 ~ 60 Hz,物料溫度為 60-80 ℃(根據物料溫度調節風機頻率),濾袋抖動時間為 60 s,濾袋抖動間隔時間為10 s。選擇濃縮液密度、料液比例(輔料蔗糖粉糊精與濃縮液比例)、進風溫度、噴液流量、霧化壓力、干燥時間作為考察因素。因素和水平結果見表 1 。
表 1 一步制粒因素及水平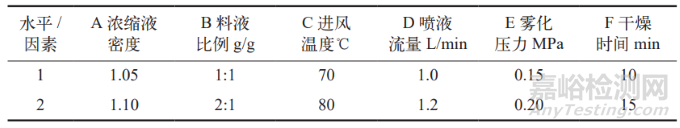
2.3 實驗結果
采用 L8(27)進行正交試驗,以顆粒的粒度和水分作為考察指標。顆粒粒度不能通過一號篩(10 目)的大顆粒與能通過五號篩(80 目)的細粉總和不得超過 8.0%,顆粒水分不得高于4.0%。試驗安排及結果見表 2,顆粒粒度方差分析結果見表 3,顆粒水分方差分析結果見表 4。
表 2 一步制粒正交試驗結果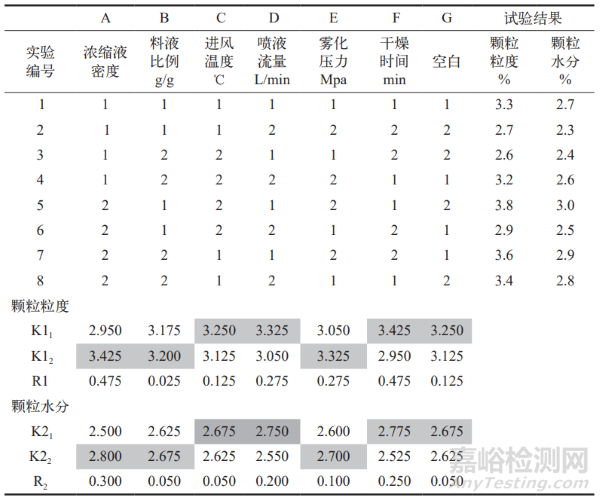
表 3 顆粒粒度方差分析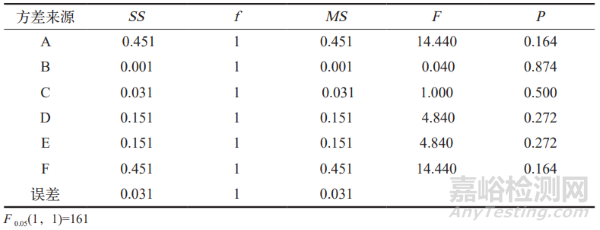
表 4 顆粒水分方差分析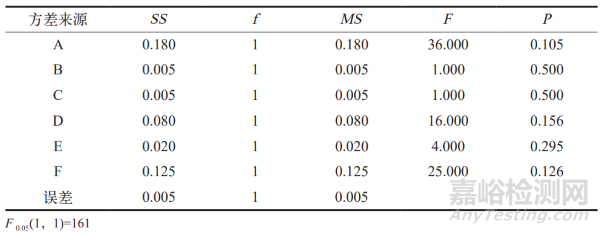
2.4 結果分析
經直觀方差分析,實驗結果表明顆粒粒度、顆粒水分均在標準要求范圍內。顆粒粒度受因素 A 和 F 的影響最大,影響順序為 A 和 F > D 和 E > C> B。顆粒水分受因素 A 的影響最為顯著,影響順序為 A > F > D > B 和C > E。綜合考量,最佳的一步制粒工藝為 A2B2C1D1E2F1。
3.中試驗證
3.1 中試方法
將制備顆粒 32 kg 處方量中藥材進行提取濃縮。取薄荷 1200 g、荊芥穗 4000 g、紫蘇葉 1200 g,這三味藥材加入 10 倍量的蒸餾水以收集揮發油,之后密閉保存備用。水溶液通過100 目的濾網過濾后備用。藥渣與防風 2000 g、柴胡 2000 g、葛根 2000 g、桔 梗 1200 g、苦杏仁 1600 g、白芷1200 g、苦地丁 4000 g、蘆根 3200 g 等八味藥材進行兩次提取,第一次加 10倍量水,提取 2 h ;第二次加水 8 倍量,提取 1 h。兩次提取液均通過 100 目的濾網過濾,然后將兩次提取液與水溶液合并,減壓濃縮至密度為 1.1 后備用。
按按一步制粒頂噴技術參數和操作程序操作。設定風機頻率為 20 ~ 60 Hz,物料溫度控制在60 ~ 80 ℃(根據物料溫度調節風機頻率),濾袋抖動時間為 60 s,濾袋抖動間隔時間為 10 s。濃縮液密度設定為 1.1(保溫使用),輔料蔗糖粉 3 份與糊精 1份混合,與濃縮液的比例為 2:1。設定進風溫度為 70 ℃,噴液流量為 1.0 L/min,霧化壓力為 0.2 MPa,干燥時間為 10 min,進行中試。連續進行 3 次一步制粒中試驗證。
3.2 合格標準
性狀:應為棕黃色的顆粒,味甜、微苦。
粒度:不能通過一號篩(10 目)的大顆粒與能通過五號篩(80 目)的細粉總和不得超過 8.0%。
水分:含水量不得超過 4.0%。
溶化性:取供試品 12 g,加熱水200 ml,攪拌 5 min 后立即檢查,應完全溶解,無焦屑或異物殘留。
鑒別:(1)在供試品色譜中,與荊芥穗對照藥材和胡薄荷酮對照品色譜相應位置上,應出現相同顏色的斑點。
(2)在供試品色譜中,與荊芥穗對照藥材色譜和對照品色譜相應位置上,應出現相同顏色的斑點。
(3)在供試品色譜中,與白芷對照藥材、防風對照藥材色譜相應位置上,應出現相同顏色熒光的斑點。
(4)在供試品色譜中,與柴胡對照藥材色譜相應位置上,日光下應顯示相同顏色的主斑點;紫外光下應顯示相同的黃色熒光斑點。
(5)在供試品色譜中,與葛根素色譜相應的位置上,應顯示相同顏色的熒光斑點。
(6)在供試品色譜中,與桔梗對照藥材色譜和對照品色譜相應位置上,應出現相同顏色的斑點。
(7)在供試品色譜中,與苦地丁對照藥材色譜和對照品色譜相應位置上,應出現相同顏色的斑點。
葛根素含量:本品每袋 12 g 中含葛根以葛根素(C21H20O9)計,不得少于 10.0 mg。
3.3 中試結果
顆粒的鑒別檢查結果均符合規定,鑒別檢查圖譜詳見圖 1。顆粒的性狀、葛根素含量等詳細檢查結果見表 5,葛根素含量檢查圖譜見圖 2。
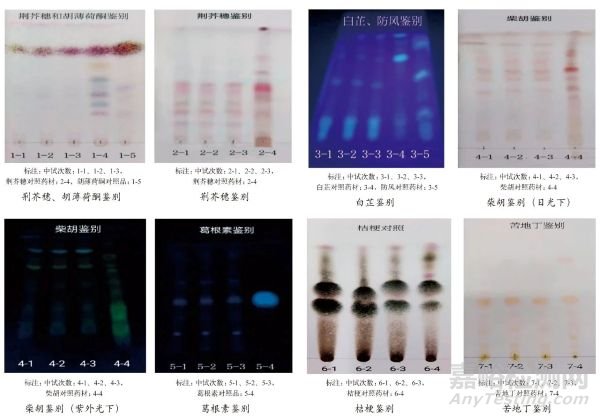
圖 1 顆粒鑒別圖譜
表 5 顆粒性狀、粒度、水分、溶化性、葛根素含量檢查結果
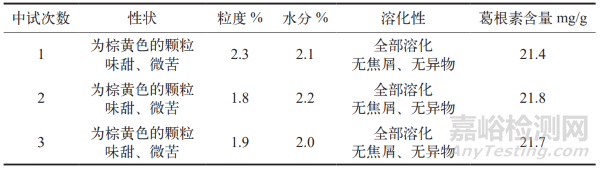
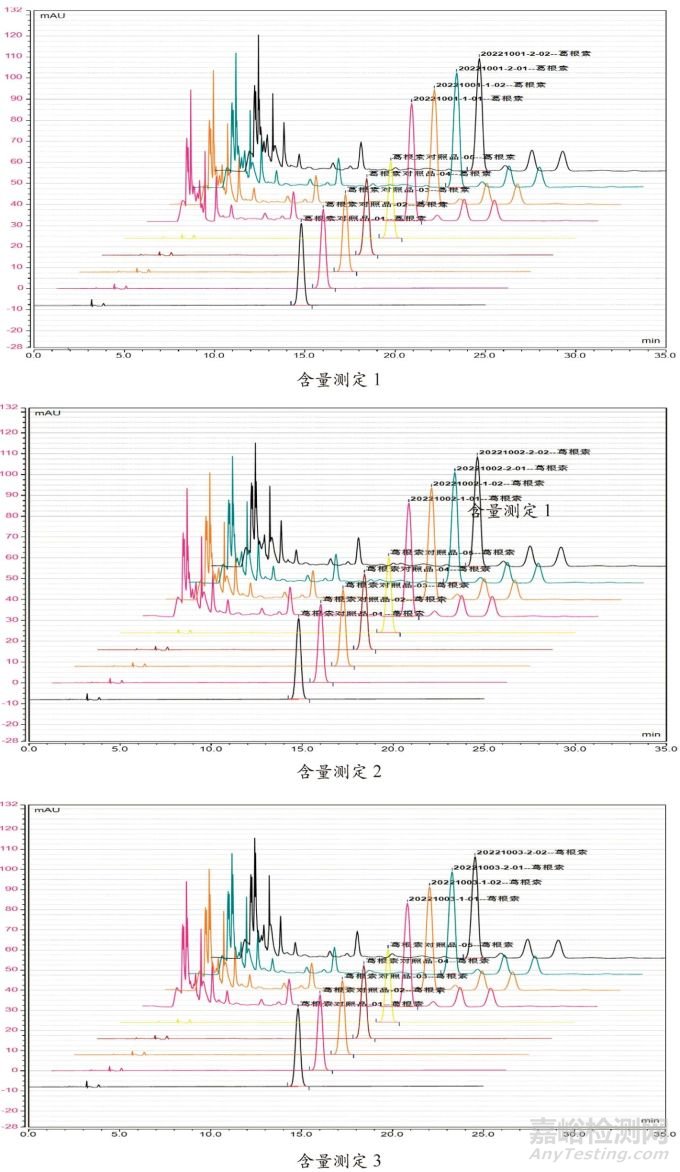
圖 2 葛根素含量測定圖譜
3.4 結果評定
經過對 3 次中試制備的顆粒進行綜合檢驗,結果表明顆粒的性狀、粒度、水分含量、溶化性能以及顆粒鑒別檢查和葛根素含量等各項指標均符合既定標準。檢驗數據之間具有較高的一致性,顯示出良好的重現性。
4.結論
感冒清熱一步制粒實驗過程發現:在濃縮過程結束后,直接對濃縮液進行保溫使用,可以減少冷藏和二次加熱等中間環節,從而節約能源并杜絕因貯存而可能滋生的微生物風險。此外,將濃縮結束的濃縮液通過 10 目篩過濾,可有效防止噴槍堵塞。在制粒前,應根據物料的溫度先設定好霧化壓力和蠕動泵的轉速,然后開始噴液和制粒。在制備過程中,應時刻注意觀察物料的沸騰狀態和成粒情況,以防止物料粘接成塊,保障生產流程的順暢。
一步制粒密閉生產方式具有諸多優點:它不僅提高了生產效率,還有效避免了細粉飛揚導致的環境污染。此外,這種生產方式減少了操作人員與有刺激性或毒性藥物及輔料接觸的機會。所制得的顆粒呈均勻細小的球狀,含水分量低,具有良好的溶解性、流動性以及含量均勻性。
本文作者張永秉1 高斌2 石朝陽3 張文標4 尚海賓5* ,1. 浙江藥科職業大學;2. 上海雷允上藥業有限公司;3. 安徽松瑞制藥有限公司;4. 河南天浩機械設備有限公司;5. 白云山湯陰東泰藥業有限責任公司,僅供交流學習。

來源:制藥工藝與裝備


