今日頭條
北京泰德AT2R拮抗劑報神經痛IND。泰德制藥針對神經病理性疼痛自主開發的TRD205創新藥的臨床試驗申請獲FDA受理。TRD205是一款血管緊張素II型2受體(AT2R)拮抗劑,采用CADD藥物設計具有全新的分子結構。在臨床前研究中,TRD205在外周神經痛、炎性疼痛和癌痛模型中均具有顯著的鎮痛作用,而且不會產生中樞相關的不良反應,安全性良好。
國內藥訊
1.派格長效GLP-1R激動劑報產。派格生物每周一次、一次性預填充自動注射筆皮下給藥的GLP-1R激動劑維派那肽注射液(PB-119 )的上市申請獲CDE受理,用于治療2型糖尿病。PB-119可作用于胰腺發揮葡萄糖濃度依賴性降低血糖作用;同時還作用于大腦、胃腸道、肝臟等多個器官,有效控制食欲、延緩胃排空、減重、降壓、調脂。PB-718有望成為顯著改善患者用藥依從性與生活質量的T2D患者治療選擇。
2.君實PD-1單抗黑色素瘤III期臨床成功。君實生物自主研發的PD-1抑制劑特瑞普利單抗一線治療不可切除或轉移性黑色素瘤的III期MELATORCH研究達到主要研究終點。與達卡巴嗪相比,特瑞普利單抗一線治療顯著延長基于獨立影像評估的無進展生存期(PFS);藥物的安全性數據與既往研究相似,未發現新的安全性信號。詳細數據將在國際學術大會上公布。
3.盟科噁唑烷酮類抗生素獲QIDP和快速通道資格。盟科藥業針對耐藥革蘭氏陽性菌感染開發的噁唑烷酮類抗生素MRX-4獲FDA授予合格傳染病產品(QIDP)和快速通道(Fast Track)資格認定,聯合康替唑胺片用于治療中重度糖尿病足感染(不伴有骨髓炎)。目前,盟科藥業正在國際Ⅲ期臨床中評估這一組合治療糖尿病足感染的有效性與安全性,該項試驗的中國部分由四川大學華西醫院冉興無教授擔任主要研究者。
4.珠海聯邦三靶點激動劑上Ⅰ期臨床。聯邦制藥自研、GLP-1R/GIPR/GCGR三靶點激動劑UBT251登記啟動Ⅰ期臨床,擬評估健康受試者單次皮下注射UBT251的安全性、耐受性、藥代動力學、藥效動力學。在臨床前多種動物模型研究中,UBT251已顯示出降低血糖和體重,改善肝臟脂肪變性和纖維化的潛力。聯邦制藥計劃開發UBT251用于治療2型糖尿病、超重/肥胖、非酒精性脂肪性肝病。
5.翰森Trop-2靶向ADC獲批實體瘤臨床。翰森制藥附屬公司翰森生物與恒邦藥業聯合申報的1類生物藥注射用HS-20105的臨床試驗獲國家藥監局默示許可,擬用于晚期實體瘤的治療。HS-20105是一款靶向Trop-2的抗體藥物偶聯物(ADC)。目前,全球范圍內僅有一款Trop-2靶向ADC藥物獲批上市,即吉利德旗下的戈沙妥珠單抗(Trodelvy)。云頂新耀擁有Trodelvy在大中華區的開發權益。
國際藥訊
1.諾華放射性配體組合療法Ⅲ期臨床積極。諾華放射性配體藥物Lutathera聯合長效奧曲肽(octreotide)一線治療生長抑素受體(SSTR)陽性、2級和3級晚期胃腸胰神經內分泌腫瘤(GEP-NETs)患者的Ⅲ期臨床NETTER-2達到主要終點。與單用高劑量octreotide相比,聯合治療顯著改善患者的無進展生存期(PFS);而且聯合用藥未觀察到新的安全性問題。詳細結果將在醫學會議上公布。
2.默沙東TL1A抗體啟動UC的Ⅲ期臨床。默沙東潛在“first-in-class”TL1A抗體MK-7240(PRA023)在Clinicaltrials.gov網站上注冊一項Ⅲ期臨床(MK-7240-001),擬評估用于治療中重度活動性潰瘍性結腸炎的有效性與安全性。在Ⅱ臨床中,PRA023治療組和對照組臨床緩解率分別為26.5%和1.5%,內窺鏡檢查改善率分別為36.8%和6.0%,臨床響應率分別為66.2%和22.4%。今年4月,默沙東以108億美元的價格收購Prometheus公司并獲得其首發管線PRA023項目。
3.漸凍癥納米療法長期療效積極。Clene公司及其子公司Clene Nanomedicine開發的創新納米療法CNM-Au8治療肌萎縮側索硬化(ALS)的臨床研究(HEALEY ALS)長期隨訪數據積極。與歷史數據集的匹配安慰劑受試者相比,CNM-Au8(30 mg)治療組患者生存期顯著改善,死亡風險降低49%(HR:0.510,95% CI:0.263-0.987,p=0.046)。CNM-Au8是一種具有催化活性、表面清潔、濃縮的金元素多面納米晶體的水懸浮液,可促進髓鞘再生和神經保護作用。
4.創新口服CETP抑制劑AD早期臨床積極。NewAmsterdam公司選擇性CETP抑制劑obicetrapib用于治療攜帶至少一個載脂蛋白E4(APOE4)變體的早期阿爾茨海默病(AD)患者的Ⅱa期臨床結果積極。24周隨訪數據顯示,患者腦脊液中24-羥基膽固醇和27-羥基膽固醇的水平分別降低了11%和12%;患者血漿中的Aβ42/40比值增加了8%,pTau181水平保持穩定。此外,obicetrapib總體耐受性良好。
5.拜耳放射性核素療法上Ⅰ期臨床。拜耳放射性核素療法BAY3546828在Clinicaltrials.gov網站上注冊首次人體Ⅰ期臨床,計劃入組140例晚期轉移性去勢抵抗性前列腺癌 (mCRPC) 受試者,評估BAY3546828(Actinium-225-macropa-pelgifatamab)的安全性、耐受性、藥代動力學和初步抗腫瘤活性。BAY3546828能夠釋放出一種傳播距離很短的放射性物質,并通過與癌細胞表面的前列腺特異性膜抗原(PSMA)的蛋白質結合以達到殺死癌細胞的目的。
6.諾和諾德27億美元開發心臟代謝疾病創新藥。諾和諾德與Valo Health公司將利用后者大型人類數據集和人工智能(AI)驅動的技術平臺,合作開發用于治療心臟代謝疾病的創新藥物,以及心血管疾病的三個臨床前候選藥物。根據協議,Valo將獲得總額為6000萬美元的預付款和潛在的近期里程碑款項,總額高達27億美元的多達11個項目的里程后期碑付款,和研發資金等費用。
醫藥熱點
1.長護險失能等級評估管理辦法出臺。為加強長期護理保險失能等級評估管理,保障參保人合法權益,國家醫保局起草《長期護理保險失能等級評估管理辦法(試行)》《長期護理保險失能等級評估機構定點管理辦法(試行)》,向社會公開征求意見。其中,文件明確不予受理失能等級評估申請的情形包括:未參加長期護理保險的;不符合待遇享受條件的;發生的護理服務費用不屬于長期護理保險基金支付范圍的;申報材料不全或提供虛假材料的;其他長期護理保險不予受理評估的。
2.中國首個人源干細胞國標發布。9月23日,第四屆中國干細胞與再生醫學協同創新平臺大會暨首屆金鳳干細胞論壇在重慶舉行,大會正式發布我國首個人源干細胞國家標準《生物樣本庫多能干細胞管理技術規范》(GB/T42466-2023)。《規范》規定了生物樣本庫中人多能干細胞和小鼠多能干細胞的管理技術通用要求,包括總則、原材料和相關數據的采集與接收、建系、復蘇和培養、冷凍與儲存、質量控制、分發和運輸的管理和技術要求。
3.中國抗癌協會中西整合白血病專委會成立。9月23日,中國抗癌協會中西整合白血病專業委員會正式成立,旨在探索白血病整合診療的創新舉措,推動中西醫結合在白血病治療領域的交叉融合與積極發展。經民主選舉,中國中醫科學院西苑醫院胡曉梅教授、北京大學人民醫院江倩教授當選為首屆主任委員;貴州中醫藥大學第二附屬醫院黃禮明、北京中醫藥大學東直門醫院郎海燕、天津中醫藥大學第一附屬醫院史哲新、江蘇省中醫院孫雪梅、浙江大學醫學院附屬第一醫院佟紅艷5位專家當選為副主任委員。
評審動態
1. CDE新藥受理情況(09月26日)
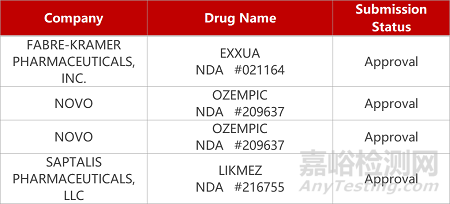
2. FDA新藥獲批情況(北美09月22日)