近期,中國醫學科學院阜外醫院潘湘斌教授和生物醫學工程研究所王偉偉教授在科愛創辦的期刊Bioactive Materials上聯合發表封面文章:完全可降解室間隔缺損封堵器。臨床所用金屬封堵器存在鎳過敏、心肌磨損和心律失常等風險。作者研發了一種完全可降解封堵器,該封堵器由聚對二氧環己酮(PDO)骨架和左旋聚乳酸(PLLA)阻流膜組成。與鎳鈦合金相比,PDO顯著緩解炎癥反應,減輕纖維化并促進內皮化。大動物室間隔缺損模型和5例患者均在超聲引導下成功植入,證實了PDO封堵器的安全性和有效性。
研究內容簡介
室間隔缺損 (VSD)是最常見的先天性心臟病之一。過去的幾十年里,經導管封堵VSD相比于開胸手術具有微創、并發癥少等優點,已成為一種優先的治療方法。目前上市的VSD 封堵器由鎳鈦合金制成。然而,永久遺留在心臟內的金屬殘留可能會導致鎳金屬過敏、心肌磨損、瓣膜損傷、傳導阻滯和血栓栓塞等嚴重并發癥,總體發生率高達0.1% ~ 8.6%,主要歸因于金屬封堵器鎳離子的長期釋放、對周圍心臟組織的持續壓迫、無法緩解的炎癥反應和延遲內皮化過程等因素。
可降解材料的出現提供了一種富有前景的方式避免體內永久金屬植入物。可降解材料,如左旋聚乳酸(PLLA)和聚二氧環己酮(PDO)具有良好的生物相容性,可在體內完全降解成二氧化碳和水,自1980年代以來已被FDA批準應用于外科縫合線和血管內支架。前期臨床試驗證明了 PLLA 和膠原兩種封堵器在房間隔缺損 (ASD) 封堵中的可行性和安全性。然而,目前可降解的封堵器保留了金屬支架提供機械支撐和增強 X 射線可見性,不能完全降解,仍然面臨金屬封堵器的上述風險。此外,與ASD相比,VSD具有更復雜的解剖結構(如更靠近房室瓣和傳導通路),血流動力學的影響更大,這對VSD可降解封堵器的形態設計、力學性能和促內皮化進程提出了更高的要求。因此,使用完全可生物降解的封堵器封堵 VSD 仍然是一項重大的臨床挑戰。
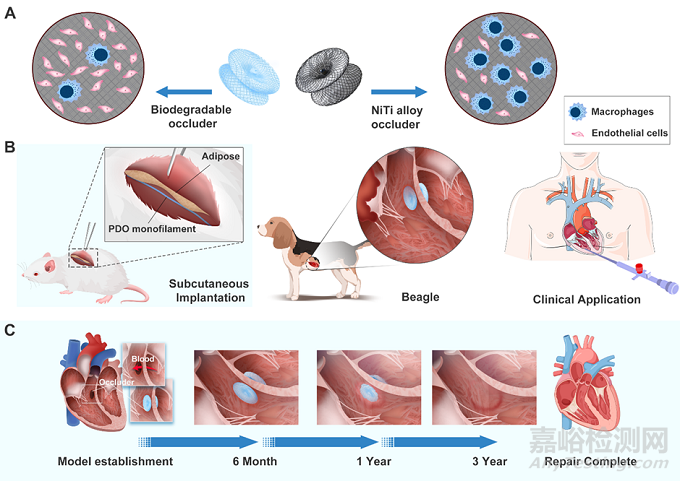
為了解決鎳鈦合金封堵器殘留在心臟的問題,作者研發了一種完全可降解的PDO封堵器,用于經導管VSD封堵 (圖1)。雙盤形PDO封堵器由骨架和阻流膜組成。結果表明,PDO具有良好的力學性能、幾何適應性、生物相容性和降解性。皮下埋植表明,與鎳鈦合金相比,PDO纖維可以顯著緩解炎癥,募集促修復M2巨噬細胞,減輕纖維化并促進內皮化。PDO封堵器超聲引導下成功植入犬VSD模型中。3年隨訪顯示PDO封堵器可誘導心臟組織再生。封堵器促內皮化進程快于降解過程,保證無殘余分流或位移發生。隨著封堵器的降解,偶發心律失常的發生頻率降低,未見致死性心律失常。在5例VSD患者的臨床試驗中,所有封堵器都在超聲引導下成功植入,3個月隨訪無殘余分流、瓣膜損傷和致命心律失常等不良事件。總之, PDO封堵器在VSD治療中表現出優于鎳鈦合金的安全性和有效性,為進一步的大規模臨床試驗提供了很大的希望。
圖1:PDO封堵器設計示意圖。(A) PDO封堵器與鎳鈦合金相比,能明顯緩解炎癥,促進內皮化。(B) PDO封堵器的安全性和有效性在大鼠皮下埋植模型、犬VSD模型和5例VSD患者的臨床試驗應用中得到驗證。(C) 犬VSD模型3年隨訪顯示了PDO封堵器誘導心臟修復的過程。
一、完全可降解室間隔缺損封堵器的制備
首先,PDO單絲通過熔融紡絲制成,將分子量為180 kDa的PDO顆粒加熱至160 °C,熔化后,從紡絲機中擠出,在水浴中冷卻,形成直徑為0.15 mm的單絲。將長度為單絲編織成網管并放入設計好的模具中,加熱至 100 °C 60 分鐘,冷卻至室溫以形成雙盤形狀。隨后將兩片厚度為0.1 mm的PLLA熔融紡絲封堵膜,激光切割成匹配的尺寸,并用PDO單絲固定在圓盤和封堵器的腰部。
PDO 材料的形狀記憶和彈性不如鎳鈦合金,這可能會導致封堵器從導管中釋放后無法復形。為加強PDO骨架的幾何適應性,作者在左側傘盤上編織了一條PDO單絲制成的塑形線。封堵器從導管中展開后,可將其收緊以壓縮和塑形傘盤。值得注意的是,作者移除了所有金屬標記,賦予了 PDO 封堵器完全的生物降解性。
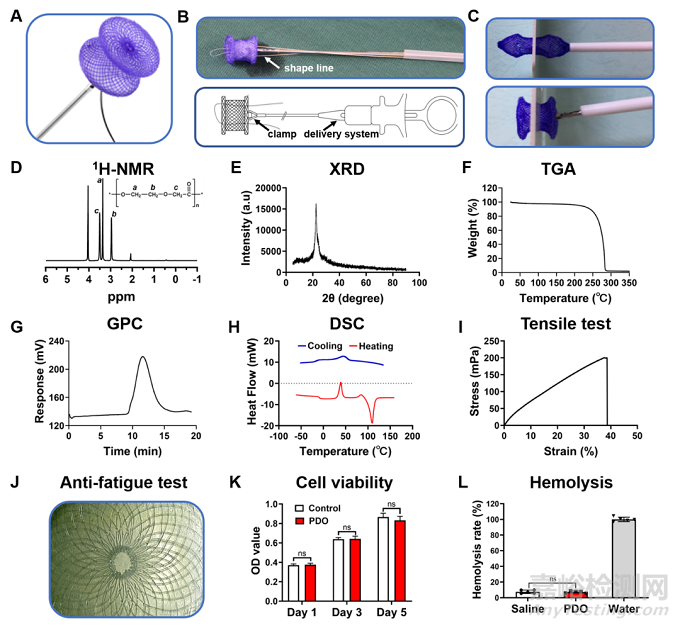
拉伸試驗的表明PDO單絲拉伸強度和斷裂伸長率分別為200.17 mPa和38.6%,符合封堵器強度需要。經過950萬次3000N負荷的疲勞試驗,PDO封堵器的結構完好無損。顯微鏡檢查未見封堵器斷裂、破裂或脫層,說明PDO封堵器能夠適應心室內的血壓,無變形和斷裂。
圖2:PDO封堵器的設計、性質、生物相容性。(A, B) PDO封堵器及輸送系統的設計。(C)成型線收緊前(上圖)和收緊后(下圖)封堵器釋放的形態。(D) 1H-NMR; (E) XRD; (F) TGA; (G) GPC; (H) DSC。(I)PDO單絲拉伸試驗。(J)抗疲勞試驗后PDO封堵器右側傘盤顯微圖像。(K) CCK-8測定生物相容性。(L) PDO溶血試驗。
二、大鼠皮下埋植評價體內炎癥、促內皮化反應
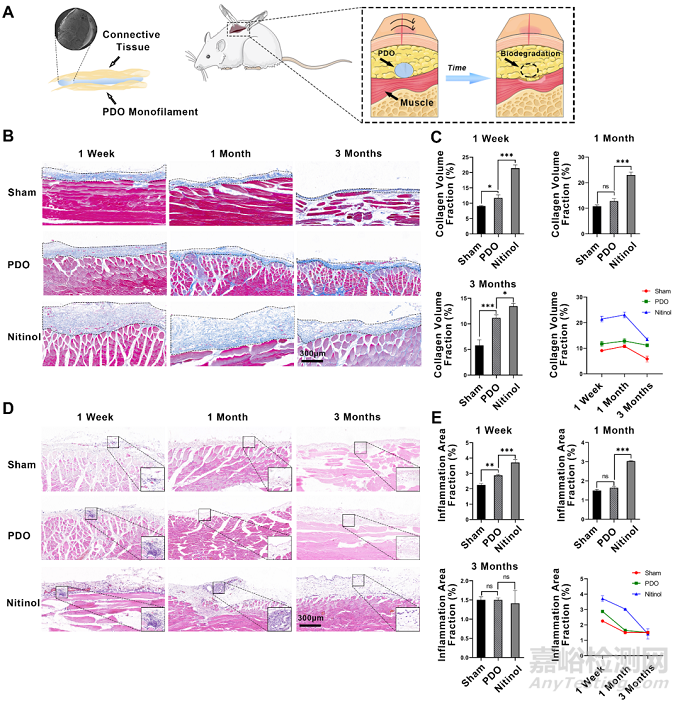
為了進一步評估體內生物相容性,將PDO單絲和鎳鈦合金植入皮下。Masson三色染色顯示,1周、1個月和3個月時,鎳鈦合金組膠原蛋白分布密度明顯高于PDO組,表明PDO引起的異物反應和纖維化包裹更輕。H&E染色進一步顯示在1周和1個月時,鎳鈦合金組中以中性粒細胞和巨噬細胞浸潤為特征的炎癥區域顯著大于PDO。這些數據表明,與鎳鈦合金相比,PDO 可以誘導強度較低且持續時間較短的炎癥反應,顯示出更好的生物相容性。
圖3:PDO在大鼠皮下埋植模型中減輕纖維化和炎癥。(A) PDO和鎳鈦合金絲皮下埋植示意圖。(B) 假手術組、PDO組、鎳鈦合金組組織分別在1周、1個月、3個月時進行Masson染色。(C) 對照組、PDO組和鎳鈦合金組膠原體積分數的統計分析 (n = 3)。(D)對照組、PDO組和鎳鈦合金組H&E染色的代表性圖像。(E) 對照組、PDO組、鎳鈦合金組炎癥面積分數統計學分析 (n = 3)。黑色虛線表示植入物和組織之間的界面。
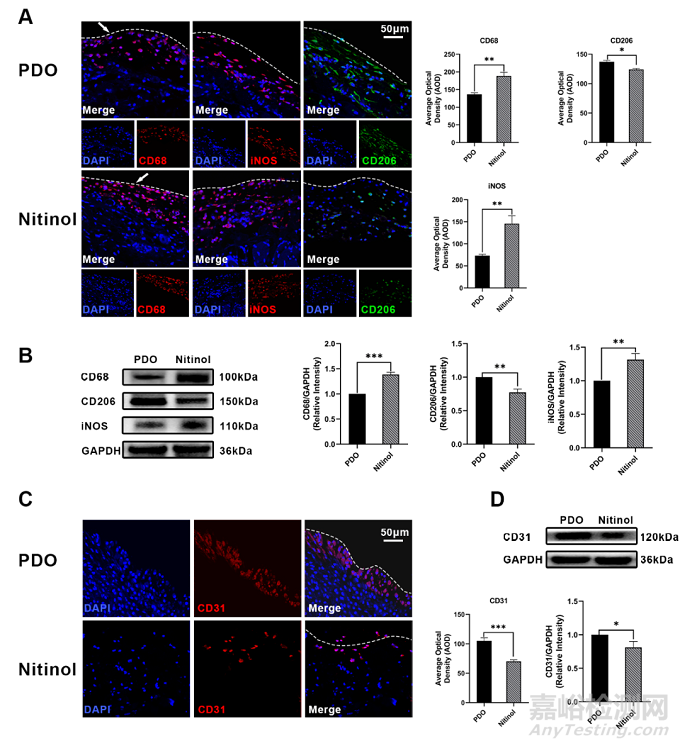
巨噬細胞在異物反應中起核心作用,與炎癥持續時間密切相關。PDO招募的巨噬細胞(CD68+)數量明顯低于鎳鈦合金組。此外,更多的M2型巨噬細胞在PDO組中極化,表明PDO誘導促修復過程。免疫組化和WB進一步驗證,CD68和iNOS的表達在鎳鈦合金組中顯著上調,而CD206在PDO組中上調。這些結果表明PDO促進了體內的修復反應。
可生物降解材料有利于細胞粘附和浸潤,可促進內皮化進程。與鎳鈦合金相比,PDO在1個月時顯著增加了CD31+內皮細胞的浸潤。WB顯示CD31的表達水平在PDO組也顯著上調,表明PDO有利于內皮細胞的粘附和浸潤,可促進體內內皮化進程。
圖4:PDO促進M2巨噬細胞極化和內皮化。(A) 1個月植入后CD206、CD68、iNOS免疫熒光染色,測量平均光密度(AOD) (n=3)。(B) Western blotting檢測組織中CD68、CD206和iNOS蛋白表達水平 (n=3)。(C) 1個月時組織中CD31免疫熒光染色(n=3)。(D)組織中CD31蛋白表達水平(n=3)。白色虛線表示植入物和組織之間的界面。
三、犬VSD模型3年隨訪評價封堵器安全性和有效性
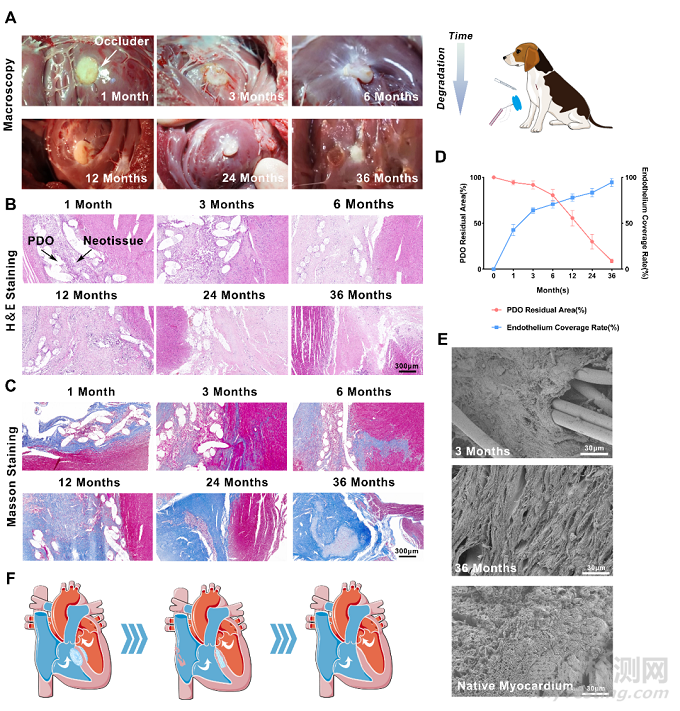
對于臨床轉化,作者進一步評估PDO封堵器在犬VSD 模型中的安全性和有效性。VSD通過穿刺室間隔和球囊擴張產生。在超聲指導下經導管植入封堵器。所有封堵器都在第一次嘗試中成功植入。第 1、3、6、12、24 和 36 個月時,3 只犬安樂死以評估PDO 封堵器體內情況。在大體檢查中,封堵器在室間隔中的位置很好,無移位,封堵器表面未見血栓。隨訪過程中,PDO封堵器殘留面積逐漸減少,內皮逐漸覆蓋傘盤,提示存在降解和內皮化過程。
H&E染色顯示隨訪期間心臟未發生嚴重炎癥、血栓或心肌磨損。6 個月內觀察到中度炎癥反應。Masson染色顯示內皮細胞從PDO邊緣向封堵器的中心生長,膠原圍繞著PDO形成。掃描電子顯微鏡顯示PDO在3個月內保持內皮細胞包圍,在36個月時完全降解,重建高度纖維化的微觀結構,類似于天然心肌的結構。
圖5:PDO封堵器植入犬VSD模型的安全性和有效性。(A) 1、3、6、12、24、36個月植入PDO封堵器的大體病理圖。(B) H&E染色。(C)Masson染色。(D) PDO殘留面積和內皮覆蓋曲線。(E) 植入封堵器3個月和36個月時掃描電鏡。(F) 降解和組織再生過程的示意圖。
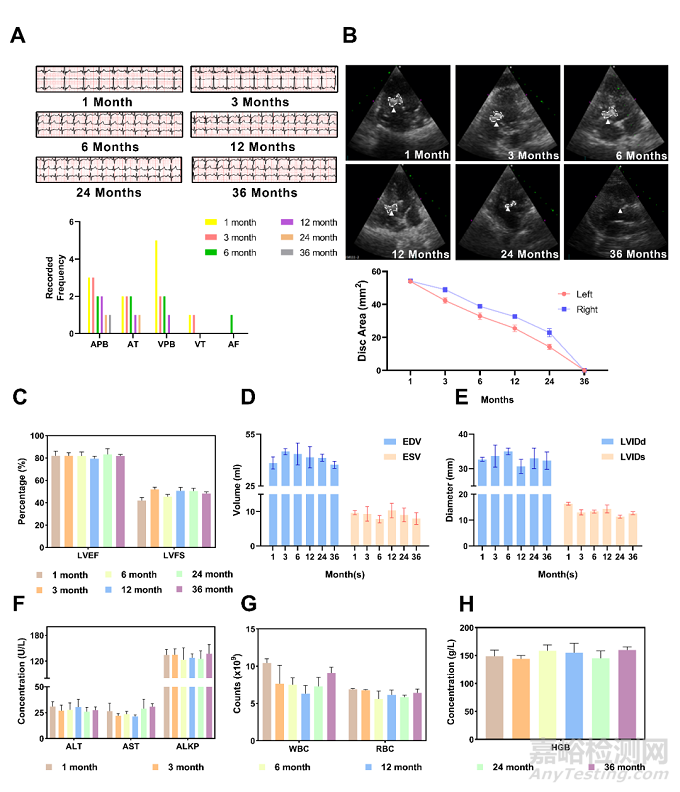
隨訪期間未觀察到致命的心律失常。隨著封堵器的退化,心律失常總頻率隨時間降低。超聲顯示封堵器處于良好位置并逐漸降解。心功能及形態均在正常范圍內,血液檢查和肝臟檢查均未發現異常,表明 PDO封堵器在長期隨訪期間無毒性。
圖6:犬VSD模型的心電圖、超聲和血液檢查。(A) 隨訪時心電圖代表性圖像。(B) 超聲圖像及左右傘盤降解分析。白色虛線勾勒為封堵器輪廓。(C-E)超聲心動圖定量LVEF、LVFS、LVEDV、LVEDS、LVIDd和LVIDs (n=3)。(F-H) 血常規及生化常規檢查 (n=3)。
四、5例VSD患者臨床應用
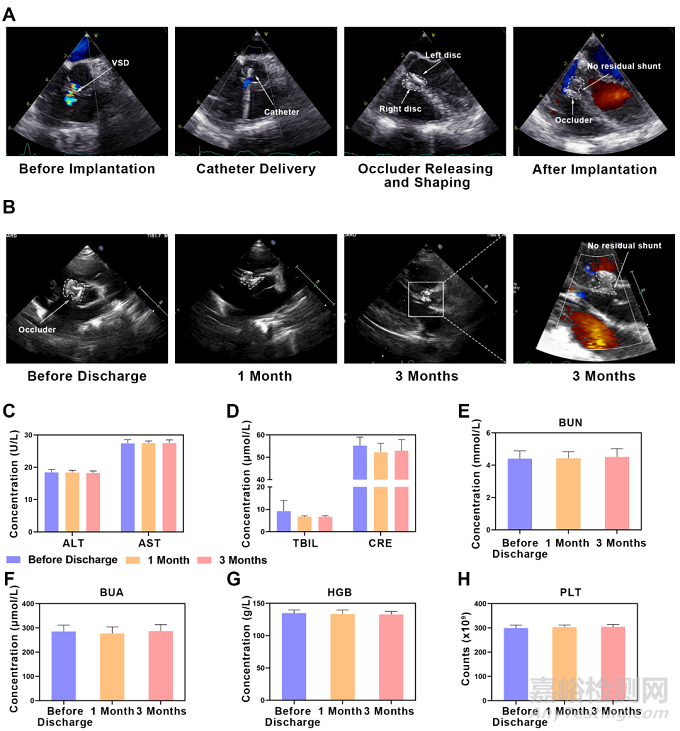
為了進一步評估封堵器的安全性和有效性, 2020 年 4 月至 2020 年 7 月對 5 名膜周部 VSD 患者進行了超聲引導下經導管植入。所有封堵器均成功植入。沒有發生心臟驟停、主動脈或三尖瓣反流加重、心包積液或心包填塞等主要不良事件。
圖7:PDO封堵器在VSD患者中的臨床應用。(A) 超聲指導下PDO封堵器植入手術。(B) 超聲隨訪3個月結果。(C-H) 血常規及生化常規檢查(n = 5)。
綜上所述,PDO封堵器具有生物相容性、機械穩定性、降解性、緩解炎癥反應和促進內皮化等優點,是一種富有前景的先心病治療方式。作者預期PDO封堵器在未來的大規模臨床試驗中可以顯示出安全性和有效性。
原文信息:
Li Z, Kong P, Liu X, Feng S, Ouyang W, Wang S, Hu X, Xie Y, Zhang F, Zhang Y, Gao R, Wang W, Pan X.
A fully biodegradable polydioxanone occluder for ventricle septal defect closure.
Bioactive Materials, 24 (2023) 252-262.